| 제목 | [기술분석] 신약 연구 개발 과정 및 최신 미국 동향 |
|---|
| 분류 | 생명공학/바이오 | 판매자 | 강정훈 | 조회수 | 228 | |
|---|---|---|---|---|---|---|
| 용량 | 1.03MB | 필요한 K-데이터 | 5도토리 |
| 파일 이름 | 용량 | 잔여일 | 잔여횟수 | 상태 | 다운로드 |
|---|---|---|---|---|---|
| 1.03MB | - | - | - | 다운로드 |
| 데이터날짜 : | 2023-04-11 |
|---|---|
| 출처 : | 국책연구원 |
| 페이지 수 : | 14 |
< 목 차 >
I . 개요
Ⅱ. 신약 연구 개발과 승인 절차
Ⅲ. 임상시험
Ⅳ. R&D 파이프라인
Ⅴ. 제약 및 생명공학 R&D 자금 지원
Ⅵ. 결론
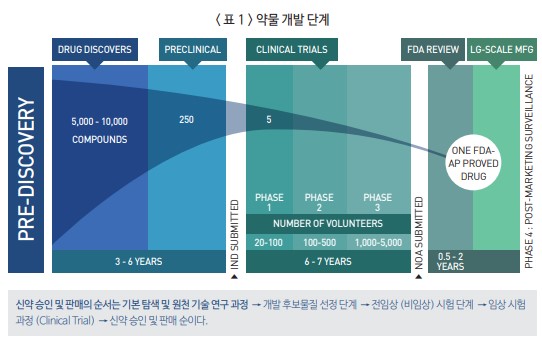
⊙ 신약개발 프로세스는 역동적인 연구와 개발이 같이 진행 되는 복합적인 과정이지만 간략하게 연구와 개발 단계로 볼수있다. 기초 연구시, 타겟하고자 하는 질병을 정하고, 기초물질의 발견 및 합성 여부, 안정성 및 효능을 테스트하는 과정이다. 이때, 반복적인 전임상 동물연구를 통해 유력한 후보 물질이나 물질들이 선정된다. ⊙ 개발 단계는 도출된 후보물질에 대한 제형 특성의 심층 연구, 체내 안정성과 안전성, 신진대사와 질병에 따른 인체내 동력학적 연구와 시험 (ADME (Absorption, Distribution, Metabolism and Excretion)), 배출후 안전성(environmental safety upon Elimination), 대규모 생산 공정 개발, 임상 1, 2, 3상 시험을 실행한다⊙ 표 1은 하나의 신약 개발과 승인 기준, 전반적인 개발후보물질 선정과 전(비)임상/임상 시험, 승인, 판매에 소요되는 비교적 데이타와 필요한 시간을 보여준다. 전임상 시험결과를 기반으로 FDA 에 임상시험 개시를 위한 IND (Investigational New Drug) 승인 전 까지는 대략 3-6년의 시간이 소요된다. ⊙ IND 요구시, 필요한 자료는 다음과 같다: (1) 전임상 시험 결과 와 설명 (absorption, distribution, metabolism, and excretion(ADME) 동물 시험 결과 포함), (2) 향후 연구 진행 계획 과 (3)관련 문헌들. 미국 FDA는 30일 이내에 IND를 검토해야 하고, 승인이 되면 임상시험을 시작 할 수 있다. 여기에 식약처의 시간은 U.S. FDA에 기준한 시간이며 문제가 재기될시 30일 이상이 된다. ⊙ 임상시험 소요 기간은 보편적, 전체질환 기준으로 약물개발과 전임상은 대략 3-6년, 임상시험은 임상 1상 착수부터 승인까지 약 8-10년 소요된다. 임상 1상의 약물의 안정성 확인, 임상 2상의 약물의 유효성 확인 그리고 마지막 임상 3상에서는 환자에 대한 약물효과와 안전성확인을 하게 된다. 모든 임상실험이 완료되면 0.5-2년 후에 최종승인을 받게 된다. ⊙ 근래, 2021년 처음 출시된 84개의 신규 활성 물질 (New Active Substance, NAS)은 5년 전에 비해 두배가 넘는 숫자이고, 지난 20년간 총 출시된 물질은 883건으로 늘어났다.1) 특히, 항암 신규 활성 물질의 수는 30개로, 최근 10년 중 최다 기록을 갱신했다. 그 뒤로 신경, COVID-19, 심장, 면역 관련 물질들의 출시가 많이 되었다. (그림 1) ⊙ 미국은 가장 빠르고 가장 많은 신규 활성 물질을 출시한 국가이며, 2021년 출시된 NAS 72개 중 44개(60% 이상)가FDA에 의해 1등급으로 분류되었다.
※ 본 서비스에서 제공되는 각 저작물의 저작권은 자료제공사에 있으며 각 저작물의 견해와 DATA 365와는 견해가 다를 수 있습니다.

