| 제목 | [산업분석] 2023년 FDA 신약 승인 현황 |
|---|
| 분류 | 생명공학/바이오 | 판매자 | 안소영 | 조회수 | 56 | |
|---|---|---|---|---|---|---|
| 용량 | 525.39KB | 필요한 K-데이터 | 5도토리 |
| 파일 이름 | 용량 | 잔여일 | 잔여횟수 | 상태 | 다운로드 |
|---|---|---|---|---|---|
| 525.39KB | - | - | - | 다운로드 |
| 데이터날짜 : | 2024-01-15 |
|---|---|
| 출처 : | 국책연구원 |
| 페이지 수 : | 11 |
[Overview]
2023년 한 해 동안 미국 FDA는 총 55개의 신약을 승인했다(CDER 기준). 이는 2022년 승인 건수(총 37건) 대비 약 50% 증가한 수치다.
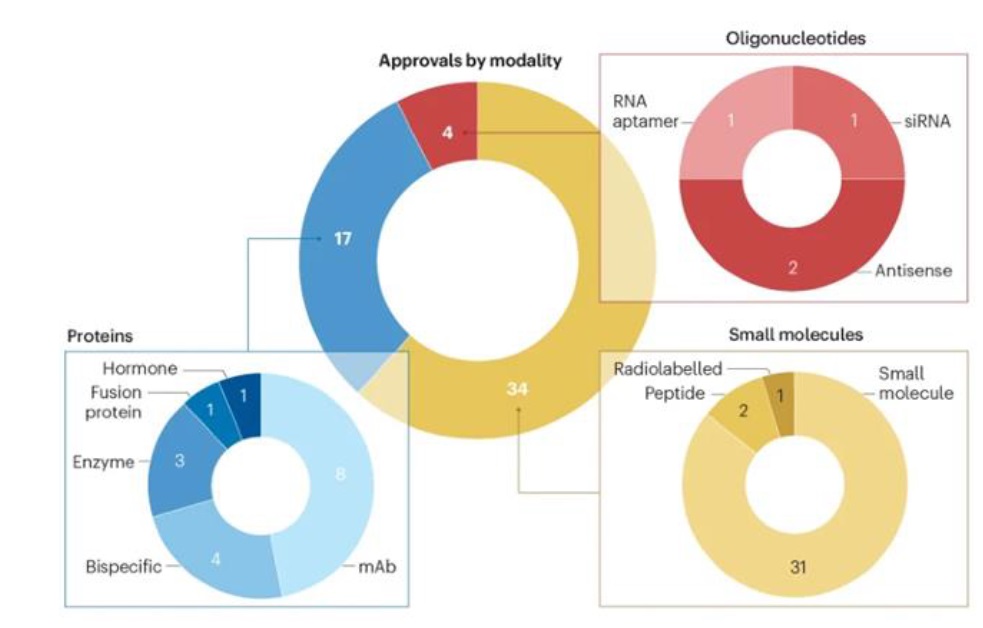
적응증 유형별로는 Oncology(13건), Neurology(9건), Infectious diseases & Haematology(각 5건)의 순으로 승인 되었으며, 모달리티 유형별로는 Small molecules(34건), Proteins(17건), Oligonucleotides(4건) 순으로 승인 되었다.
이번 자료에서는 네이처 리뷰지에서 공개한 2023년 승인 신약(55건)과 거절된 신약(9건), 올해의 주목할 만한 파이프라인(19건)을 소개한다.
1. 2023년 FDA 승인 현황
2023년 FDA는 의약품 평가연구센터(Center for Drug Evaluation and Research, CDER)에서 55개, 생물의약품 평가연구센터(Center for Biologics Evaluation and Research, CBER)에서 16개로 총 71개의 신약을 승인하였다. 앞선 2022년의 FDA 승인 건수가 총 45건(CDER: 37, CBER: 8건)인 것에 비교하였을 때, 23년의 신약 승인은 크게 증가하였다.
----------------------------------------------------------------------------------------------------------------------------------------------------
※ 본 서비스에서 제공되는 각 저작물의 저작권은 자료제공사에 있으며 각 저작물의 견해와 DATA 365와는 견해가 다를 수 있습니다.

